W chemii pojęcie "układ" odgrywa kluczową rolę, ponieważ odnosi się do zbioru substancji oraz ich interakcji, które chemicy analizują w danym badaniu lub eksperymencie. Można zauważyć, że układ może być naprawdę różnorodny: zaczynając od prostych roztworów, przez złożone reakcje chemiczne, aż po większe systemy, takie jak układy biologiczne. Warto także zwrócić uwagę na to, że wyróżniamy różne typy układów, na przykład układy otwarte, zamknięte i izolowane. Każdy z nich działa na innych zasadach, dlatego zrozumienie tych różnic staje się kluczowe dla każdego chemika, ponieważ to one w szczególny sposób wpływają na przebieg reakcji oraz efekty, które z nich wynikają.
- Pojęcie "układ" w chemii odnosi się do zbioru substancji oraz ich interakcji w badaniach chemicznych.
- Układy mogą być różnorodne, w tym otwarte, zamknięte i izolowane, co wpływa na ich działanie oraz przebieg reakcji.
- Układ otwarty umożliwia wymianę masy i energii z otoczeniem, jak gotowanie wody w otwartym garnku.
- Układ zamknięty pozwala na wymianę energii, ale nie masy, przykładem jest zakorkowana probówka.
- Układy izolowane nie prowadzą wymiany ani masy, ani energii, jak termos.
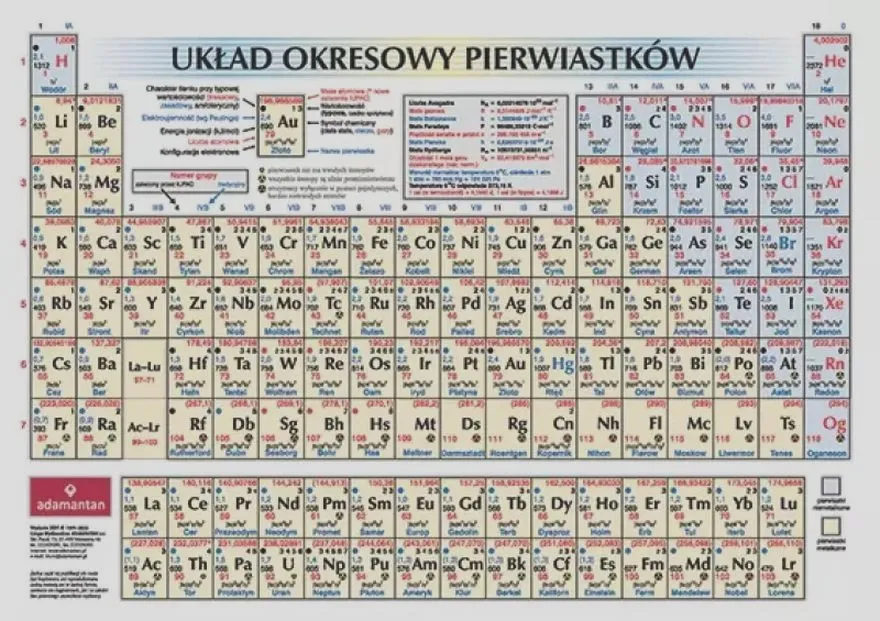
- Układ okresowy pierwiastków jest kluczowym narzędziem w chemii, organizującym informacje o pierwiastkach.
- Równowaga chemiczna występuje, gdy stężenia reagentów i produktów pozostają stałe w zamkniętym układzie.
- Wizualizacja układów chemicznych umożliwia zrozumienie złożonych procesów na poziomie atomowym i molekularnym.
Gdy przyjrzymy się konkretnym przykładom układów w chemii, sytuacja staje się jeszcze ciekawsza. Przykładowo, w układzie otwartym zachodzi wymiana masy i energii z otoczeniem — doskonałym przykładem może być gotowanie wody w otwartym garnku, gdzie para wodna swobodnie opuszcza granice układu. Z drugiej strony, układ zamknięty, taki jak butelka gazu, pozwala na wymianę energii, ale nie masy z otoczeniem, co stanowi istotne ograniczenie. Jeśli natomiast weźmiemy pod uwagę układy izolowane, to idealnym przykładem będzie termos, w którym zarówno masa, jak i energia pozostają w obrębie systemu. Poznanie tych koncepcji nie tylko fascynuje, ale również stanowi fundament dla badań chemicznych oraz zrozumienia zjawisk zachodzących w naszym otoczeniu!
Rodzaje układów chemicznych: układy otwarte
Układy otwarte fascynują swoim złożonym charakterem, co sprawia, że zasługują na szczegółowe omówienie. Czym właściwie są te układy? Przede wszystkim chodzi o systemy, które swobodnie wymieniają zarówno energię, jak i materię z otoczeniem. Aby lepiej zobrazować to zagadnienie, warto sięgnąć po przykład zwykłej probówki, w której prowadzi się reakcje chemiczne. Na przykład, kiedy dokonamy rozkładu węglanu wapnia, generujemy gaz (CO2), który bez przeszkód wydostaje się na zewnątrz, pod warunkiem, że probówka pozostaje otwarta. Taki proces doskonale ilustruje działanie układu otwartego w praktyce, a także umożliwia aktywną wymianę podczas rozwoju różnych reakcji chemicznych, zarówno w laboratoriach, jak i w przyrodzie.
Warto również zwrócić uwagę na to, że układy otwarte stanowią przeciwieństwo układów zamkniętych, które dopuszczają jedynie wymianę energii z otoczeniem. A co w przypadku układów izolowanych? Tam nie dochodzi do wymiany ani materii, ani energii. Zrozumienie tych różnic odgrywa kluczową rolę w pracy każdego chemika. Otwarte układy odgrywają zatem istotną rolę w badaniach chemicznych, ponieważ reagują na wszelkie zmiany w swoim otoczeniu, co czyni je idealnymi do obserwacji zjawisk termodynamicznych. Różnorodność typów układów umożliwia nam badanie szerokiego wachlarza procesów, począwszy od prostych reakcji w probówkach, poprzez bardziej złożone interakcje w skali przemysłowej. To właśnie te zmiany i interakcje pozwalają nam na głębsze zrozumienie zjawisk chemicznych, które nas otaczają.
| Cecha | Opis |
|---|---|
| Definicja | Systemy, które swobodnie wymieniają zarówno energię, jak i materię z otoczeniem. |
| Przykład | Rozkład węglanu wapnia w otwartej probówce generujący gaz CO2. |
| Rola w badaniach chemicznych | Reagują na zmiany w otoczeniu, idealne do obserwacji zjawisk termodynamicznych. |
| Przeciwieństwo | Układy zamknięte - wymiana energii, ale nie materii; układy izolowane - brak wymiany zarówno energii, jak i materii. |
| Znaczenie | Umożliwiają badanie różnorodnych procesów chemicznych od prostych reakcji do złożonych interakcji przemysłowych. |
Ciekawostką jest to, że układy otwarte są kluczowe dla zrozumienia procesów biologicznych, takich jak oddychanie czy fotosynteza, gdzie wymiana materii i energii z otoczeniem jest niezbędna do funkcjonowania organizmów żywych.
Rodzaje układów chemicznych: układy zamknięte
Układy zamknięte w chemii stanowią niezwykle interesujący temat, który przyciąga uwagę zarówno studentów, jak i doświadczonych chemików. A skoro już tu trafiłeś to poznaj zasady działania korozji i dowiedz się, jak jej unikać. W tego rodzaju układach obserwujemy sytuację, w której energia może wymieniać się z otoczeniem, natomiast materia nie ma takiej możliwości. Rozważmy klasyczny przykład zakorkowanej probówki, w której zachodzi reakcja chemiczna. Wprowadzając węglan wapnia (CaCO₃), po pewnym czasie zauważamy wydzielający się dwutlenek węgla (CO₂). Kiedy probówka jest otwarta, gaz swobodnie opuszcza układ. Jednak gdy zatykamy probówkę, przekształcamy ją w układ zamknięty, w którym energia (w postaci ciepła bądź ciśnienia) może się przenosić, ale pozostałe substancje pozostają „w więzieniu” probówki.
Oprócz tego, układ zamknięty można zaobserwować w komorze reakcyjnej w laboratoriach, gdzie przeprowadza się reakcje chemiczne z zachowaniem wszystkich produktów reakcji wewnątrz zamkniętej przestrzeni. W takich warunkach kontrolowanie procesów energetycznych oraz monitorowanie zmian ciśnienia czy temperatury staje się o wiele łatwiejsze. Należy dodać, że w układach zamkniętych można przeprowadzać różnorodne badania termochemiczne. Dzięki nim uzyskujemy precyzyjne pomiary energii reakcji w warunkach niezmiennych. Tak więc, chociaż materiały nie są wymieniane, energia swobodnie przepływa, co czyni te układy idealnymi do eksploracji zjawisk chemicznych.
Poniżej przedstawiono główne cechy układów zamkniętych:
- Brak wymiany materii z otoczeniem
- Przenoszenie energii w postaci ciepła lub ciśnienia
- Możliwość przeprowadzania badań termochemicznych
- Kontrola warunków reakcji (ciśnienie, temperatura)
Rodzaje układów chemicznych: układy izolowane
W świecie chemii układy izolowane pełnią kluczową rolę. Mamy do czynienia z systemami, które nie wymieniają ani materii, ani energii z otoczeniem. Można je graficznie przedstawić jako idealnie zamknięte pudełka. Jednak w praktyce takie układy rzadko występują, ponieważ nawet najmniejsze nieszczelności mogą prowadzić do wymiany ciepła lub cząsteczek z otoczeniem. Doskonałym przykładem układu izolowanego jest termos, w którym staramy się utrzymać temperaturę napoju przez dłuższy czas. Choć w rzeczywistości większość układów chemicznych nie osiąga 100% izolacji, warto poznać to pojęcie. Stanowi ono fundament wielu bardziej złożonych zagadnień w chemii.
W termodynamice układy izolowane zyskują szczególne znaczenie, ponieważ analizuje się w nich różnorodne procesy energetyczne. Na przykład, możemy rozważać zmiany entropii w układzie izolowanym, który nie wymienia ciepła z otoczeniem. Taki kontekst pozwala lepiej zrozumieć zasady rządzące procesami fizycznymi i chemicznymi. Dodatkowo, badając reakcje chemiczne w układzie izolowanym, z łatwością identyfikujemy zmiany energii swobodnej, co okazuje się kluczowe przy określaniu kierunku reakcji. W teorii, układ izolowany umożliwia przeprowadzanie symulacji w idealnych warunkach, co może być nieocenione w przypadku bardziej skomplikowanych układów, takich jak układy otwarte czy zamknięte. To właśnie te podstawowe pojęcia stanowią punkt wyjścia do dalszych eksploracji w fascynującym świecie chemii!
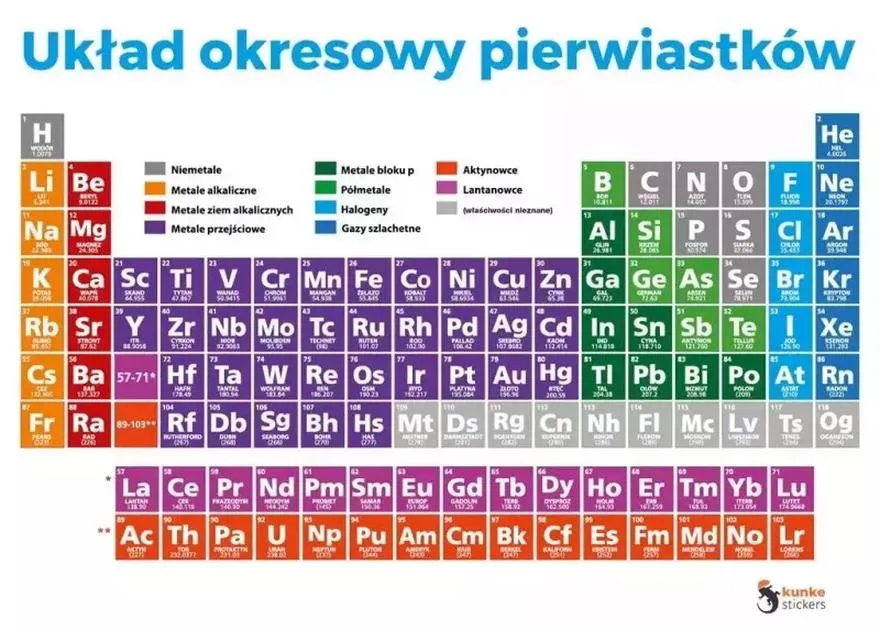
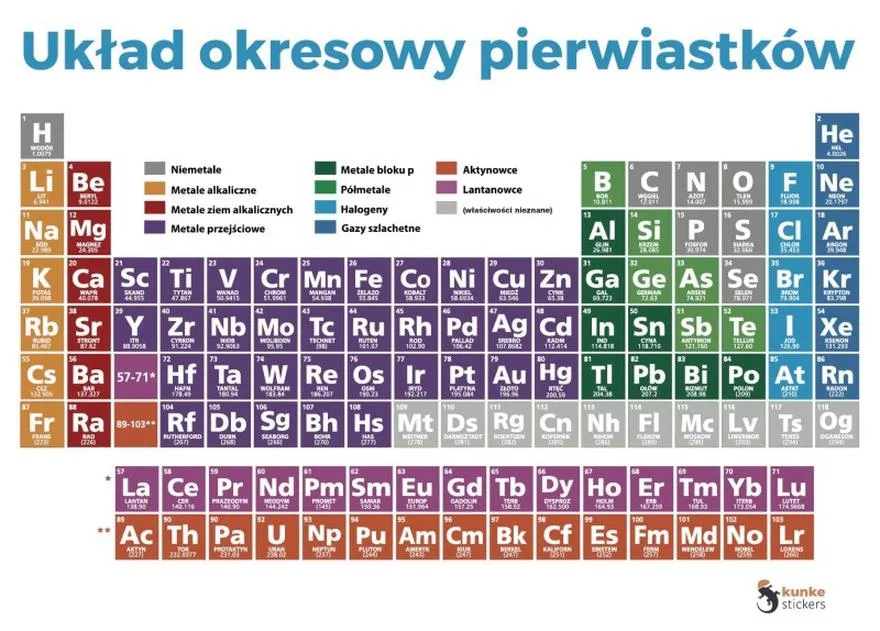
Układ okresowy pierwiastków: kluczowe narzędzie w chemii
Układ okresowy pierwiastków stanowi prawdziwy skarb w arsenale chemików oraz entuzjastów nauki. Ta uporządkowana tablica, złożona z 118 znanych pierwiastków chemicznych, powstała z myślą o szybkim odnalezieniu kluczowych informacji, takich jak liczba atomowa, masa atomowa oraz typ bloku elektronowego. Struktura układu jest przejrzysta: pierwiastki uporządkowano według liczby atomowej, a poziome rzędy stanowią okresy, które ukazują liczbę powłok elektronowych. Z kolei pionowe kolumny, zwane grupami, prezentują pierwiastki o podobnych właściwościach chemicznych. Na przykład, kiedy przyglądam się grupie 1, obejmującej aktywne metale alkaliczne, od razu dostrzegam, że sód (Na) łatwo oddaje elektron, co czyni go idealnym kandydatem do reakcji z chlorem (Cl), który łatwo akceptuje go, tworząc sól kuchenną (NaCl).
Patrząc na kontekst praktyczny, układ okresowy okazuje się niezastąpiony zarówno w laboratoriach, jak i w przemyśle. Zrozumienie trendów okresowych, takich jak promień atomowy czy energia jonizacji, pozwala na przewidywanie reaktywności pierwiastków oraz planowanie syntez chemicznych. Na przykład, aktywność metali wzrasta w grupach z góry w dół, co sprawia, że ces (Cs) jawi się jako najbardziej reaktywny metal. Niezwykle istotne jest również to, że układ okresowy wspiera nie tylko naukę, ale także projektowanie nowych materiałów czy leków w farmacji. Jako pasjonat chemii dostrzegam, że wiedza na temat układu okresowego może zrewolucjonizować nasze podejście do nauki oraz zrozumienia coraz bardziej złożonego świata chemii. Jak już tu wpadłeś, odkryj fascynujące właściwości O2 w chemii. To narzędzie łączy teorię z praktyką, wciągając nas w fascynującą podróż po zaczarowanym królestwie pierwiastków.
Równowaga chemiczna: istota stabilizacji reagentów i produktów
Równowaga chemiczna stanowi fascynujący proces, który umożliwia reagentom oraz produktom osiągnięcie stabilnego stanu w zamkniętym układzie. Wyobraźmy sobie reakcję chemiczną, która przebiega zgodnie z równaniem A + B ⇌ C + D. Kiedy rozpoczynamy naszą reakcję, stężenie reagentów A i B utrzymuje się na dość wysokim poziomie, podczas gdy stężenie produktów C i D pozostaje niskie. Z czasem, jak to często bywa w życiu, stężenia reagentów maleją, a produktów rosną. W pewnym momencie docieramy do punktu, w którym ilość reagentów i produktów nie ulega zmianie – to właśnie określana jest jako równowaga chemiczna. Mniej więcej 50% reagentów może zamienić się w produkty, a pozostałe 50% nadal występuje w postaci reagentów. Ten zjawiskowy taniec cząsteczek sprawia, że każda z nich ma do odegrania swoją unikalną rolę.
Warto także zaznaczyć, jak ważna jest stała równowagi, oznaczana symbolem K, która wyraża stosunek koncentracji produktów do reagentów w momencie osiągania równowagi. Aby lepiej to zobrazować, przyjmijmy, że w danej reakcji stężenia C i D wynoszą odpowiednio 0,8 M oraz 0,6 M, a stężenia A i B to 0,2 M i 0,4 M. Po obliczeniu K, uzyskujemy wartość 6,0 (K = (C*D)/(A*B)), co wskazuje na znacznie większą stabilność produktów w tej reakcji. Takie analizy pozwalają chemikom przewidywać zachowanie reagentów w różnych warunkach, co staje się niezwykle istotne w procesie syntezy, przemyśle oraz badaniach naukowych. Równowaga chemiczna stanowi klucz do zrozumienia wielu zjawisk chemicznych, które na co dzień kształtują nasz świat.
Poniżej przedstawiam kilka kluczowych informacji związanych z równowagą chemiczną:
- Równowaga chemiczna zachodzi, gdy szybkość reakcji w kierunku produktów równa się szybkości reakcji w kierunku reagentów.
- W stanie równowagi stężenia reagentów i produktów pozostają stałe, choć niekoniecznie są sobie równe.
- Wartość stałej równowagi K pozwala określić preferencje reakcji chemicznej między reagentami a produktami.
- Równowaga może być przesuwana w odpowiedzi na zmiany warunków zewnętrznych, takich jak ciśnienie, temperatura czy stężenie.
Wizualizacja układów chemicznych: graficzne przedstawienie procesów
Wizualizacja układów chemicznych stanowi niezwykle fascynujący aspekt chemii, ponieważ umożliwia zrozumienie złożonych procesów zachodzących na poziomie atomowym i molekularnym. Wyobraźmy sobie, że weźmiemy 100 cząsteczek wody, które w ruchu tworzą różnorodne interakcje. Dzięki graficznym reprezentacjom dostrzegamy, jak te cząsteczki łączą się, przechodzą w różnych stanach skupienia lub reagują w różnych warunkach. Rysunki oraz modele przestrzenne ułatwiają uchwycenie dynamiki tych zjawisk, czyniąc je bardziej przystępnymi i zrozumiałymi. Na przykład klasyczny model kulko-cylindryczny pokazuje nie tylko kształt cząsteczek, ale i ich wzajemne oddziaływania. Już przy 10 cząsteczkach można zaobserwować ciekawe wzorce oraz formy, które kształtują się w wyniku ich ruchu.
Warto również zwrócić uwagę na reprezentacje 3D, które zyskują na popularności, zwłaszcza w kontekście uczelni wyższych. Dzięki nim dostrzegamy różnice między izomerami oraz skomplikowane struktury białek, które mogą liczyć nawet kilka tysięcy atomów. W niektórych laboratoriach badacze wykorzystują zaawansowane programy komputerowe do symulacji tych procesów, co pozwala na eksperymentowanie z różnymi warunkami bez ryzyka utraty materiału. Podsumowując, wizualizacja układów chemicznych nie tylko ułatwia naukę, ale także inspiruje do odkrywania nieskończonych możliwości, jakie oferuje chemia.
Czy wiesz, że wizualizacje układów chemicznych mogą być tak realistyczne, że pozwalają naukowcom przewidzieć, jak nowe substancje będą się zachowywać w różnych warunkach, zanim jeszcze zostaną one stworzone w laboratorium? To zjawisko, znane jako modelowanie molekularne, jest kluczowe w przemyśle farmaceutycznym i materiałowym, gdzie zrozumienie interakcji na poziomie atomowym może prowadzić do przełomowych odkryć.